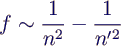Spektrum des Wasserstoffatoms
- Spektroskopie:
- Untersuchung der Frequenzverteilung von Lichtquellen
- Emissionsspektrum: Licht, das von einer angeregten
Quelle ausgeht
- Absorptionsspektrum: Licht, das beim Durchgang durch
eine Probe verändert wurde
- liefert Aufschluss über die Zusammensetzung des
Strahlers bzw. der Probe:
- analytische Chemie
- Zusammensetzung der Sterne
- Atom- und Molekülphysik
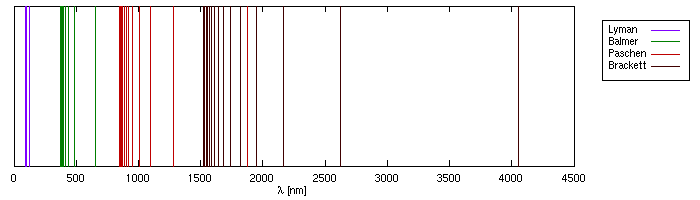
- Emissionsspektrum des Wasserstoffatoms:
- Beobachtung: Spektrum besteht aus vielen Linien, d.h.
Licht fester Frequenz:
- empirische Beziehung für die Frequenzen:
- für ganze Zahlen n < n'
- klassisch unverständlich:
- jede beliebige Bahn bzw. Energie möglich
- Elektronen auf Kreisbahnen strahlen ab → stürzen in
den Kern
- Grundidee des Bohrschen Atommodells (unhistorisch!):
- Elektron als Materiewelle mit der
deBroglie-Wellenlänge λ = h/p
- Materiewelle ist stehende Welle → nur bestimmte
Energien erlaubt
- Bahnumfang ist ein Vielfaches der Wellenlänge:
- 2 π r = n λ = n h / p = n h / (m v) für n = 1, 2,
3, ...
- ergibt mögliche Energien ("Niveaus")
- E = - (e4 m)/(8 ε02
h2) 1/n2 = -13.6 eV 1/n2 =: E0
1/n2
- für höhere Kernladungen Z erhält man entsprechend
- wesentliche Elemente fehlen im Modell (vor allem
Unschärferelation)
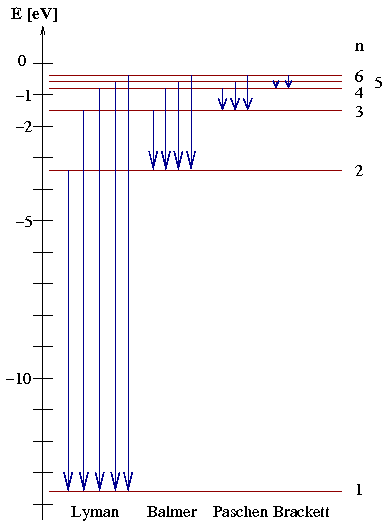
- Interpretation des Wasserstoff-Spektrums:
- Elektronen können von höheren in niedrigere
Energieniveaus übergehen
- strahlen Differenzenergie als Photon ab
- damit mögliche Linien im Spektrum bei:
- E = h f = -13.6 eV ( 1/n'2 - 1/n2
)
- in Übereinstimmung mit dem Experiment
- im Bild:
- Aufgaben: