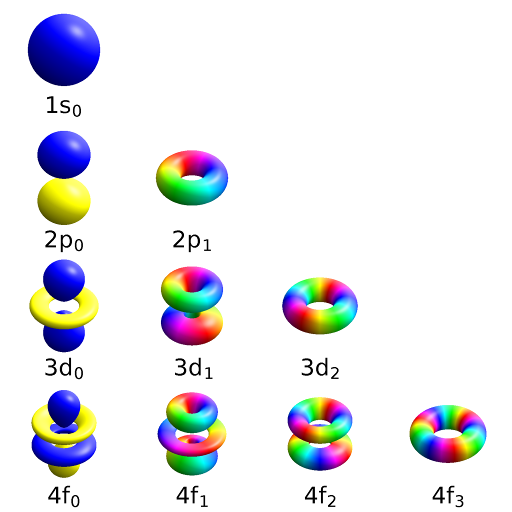
Wellenfunktionen des Wasserstoffatoms
- Lösung der Schrödingergleichung:
- ergibt gleiche Energieniveaus wie Bohrmodell
- liefert genaue Wellenfunktionen für alle Zustände
- erweitert Bohrmodell durch Bahn-Drehimpuls
- Beispiel: Wahrscheinlichkeit, das Elektron im Abstand r
vom Kern zu finden, für Grundzustand und zwei angeregte Zustände:
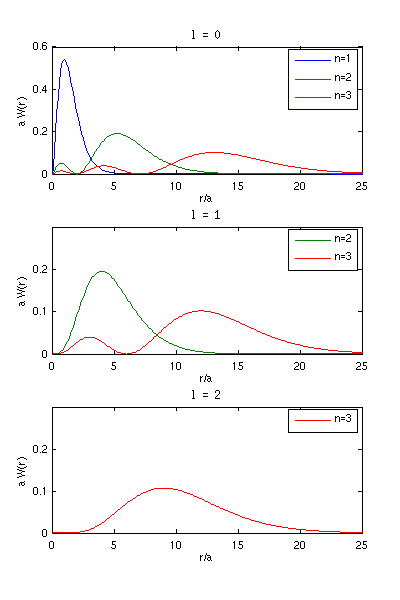
- mit dem Bohrschen Radius a = 0.529 · 10-10
m
- Bahn-Drehimpuls im Wasserstoff-Atom:
- klassisch:
- beschreibt verschieden gestauchte Ellipsen
- Vektor
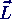 = (Lx, Ly, Lz)
= (Lx, Ly, Lz)
- senkrecht zur Bahn
- quantenmechanisch:
- Komponenten lassen sich nicht gleichzeitig messen
- nur Länge des Vektors und eine Komponente
- zur Beschreibung am besten:
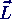 2 und Lz
(willkürlich)
2 und Lz
(willkürlich)
- ähnlich wie bei der Energie nur bestimmte Werte des Drehimpulses
möglich:
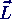 2 =
2 =  2 l (l+1)
2 l (l+1)- mit l = 0, 1, .. n-1 für Energieniveau n
- Für festen Wert l des Gesamtdrehimpulses nur bestimmte
Werte für Komponente Lz:
- Lz =
 m
m
- mit m = -l, -l+1, .., 0, 1, .. l
- Zustände des H-Atoms charakterisiert durch:
- Hauptquantenzahl n
- Werte: n = 1, 2, 3, ...
- legt die Energie des Niveaus fest
- E = E0 · 1/n2
- Grundzustandsenergie E0 = -13.6 eV
- Bahndrehimpuls-Quantenzahl l
- Werte für gegebenes n: l = 0, 1, .. n-1
- n mögliche Werte für Hauptquantenzahl n
- historische Bezeichnung: s, p, d, f, .. für l = 0,
1, 2, 3, ..
- magnetische Quantenzahl m
- Werte für gegebenes l: -l, -l+1, .., 0, .. l
- 2l+1 mögliche Werte für gegebenes l
- insgesamt n2 Zustände gleicher Energie En
(Entartung)
- Beispiele:
- Wellenfunktionen für l ≠ 0:
- von Winkeln abhängig (nicht kugelförmig)
- einige Beispiele:




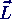 = (Lx, Ly, Lz)
= (Lx, Ly, Lz)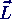 2 und Lz
(willkürlich)
2 und Lz
(willkürlich)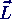 2 =
2 =  2 l (l+1)
2 l (l+1) m
m