Thermodynamische Systeme und Prozesse
-
System:
- Gegenstand oder Bereich, der zur Untersuchung als
abgegrenzt betrachtet wird.
- Das System umgibt eine gedachte oder reale Grenze,
die es vom Rest der Welt, der Umgebung, abtrennt.
- System und Umgebung wechselwirken über die
Systemgrenze hinweg, z.B. durch Wärmeübertragung, mechanische
Einflüsse oder durch Austausch von Materie.
- geschlossenes System:
kein Materie-Austausch mit der Umgebung, sonst offenes System.
- adiabates System: kein
Wärmeaustausch über die Systemgrenzen hinweg
- abgeschlossenes System:
gar keine Wechselwirkung mit Umgebung
- homogen: einheitlicher
Stoff oder Stoffgemisch. Gegenteil: heterogen (z.B. mehrere Phasen wie Wasserdampf und
Wasser). Bis auf weiteres immer homogene Systeme
-
Beispiele:
-
Inneres einer Thermosflasche
- geschlossen
- adiabat
- abgeschlossen
-
geschlossenes Becherglas mit Rührer
- geschlossen
- Wärmeaustausch mit Umgebung
(Bunsenbrenner)
- Austausch mechanischer Energie (Rührer)
-
Zylinderinneres eines Otto-Motors (Ventile vernachlässigt)
- geschlossen
- Wärmeaustausch durch Wände
- Austausch mechanischer Energie durch
Kolbenbewegung
-
Strömung durch ein isoliertes Rohr
- offen, Untersuchungsvolumen abgegrenzt
gedacht
- kein Wärmeaustausch durch Rohrwand
- kein Austausch an Zufluss und Abfluss wegen
gleicher Temperatur
- also: adiabat
-
Prozess:
- Änderung des Zustands eines Systems
- genauer auch mit Verfahren zur Änderung
-
Beispiel:
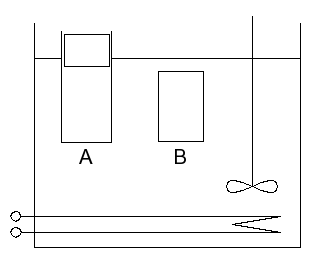
- Systemgrenzen A und B sind
wärmedurchlässig
- Temperatur des Wasserbads werde erhöht
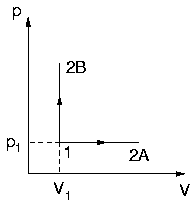
- System A: konstanter Druck, Volumen ändert
sich
- System B: konstantes Volumen, Druck ändert
sich
-
im p-V-Diagramm:
-
quasistatische Prozesse:
- Änderungen verlaufen langsam
- zu jedem Zeitpunkt kann das System als homogen und
im Gleichgewicht betrachtet werden
-
Vernachlässigung von Ausgleichsprozessen wie
- Wärmeausbreitung von der Heizung oder dem
Rührer in die System A und B
- Druckausgleich im Innern der Systeme A und
B
- schnelle Vorgänge führen zu
Nichtgleichgewichtszuständen
nicht im p-V-Diagramm darstellbar!
-
umkehrbare (reversible) Prozesse:
- System kann in den Ausgangszustand zurückgeführt
werden, ohne dass Änderungen an der Umgebung übrigbleiben
- theoretischer Grenzfall zur Vereinfachung der
Betrachtung
- Vernachlässigung von Reibungsvorgängen,
Ausgleichsvorgängen,
- führt immer über Gleichgewichtszustände
(quasistatisch)
-
Beispiel: Ausdehnung eines Gases im Wärmebad
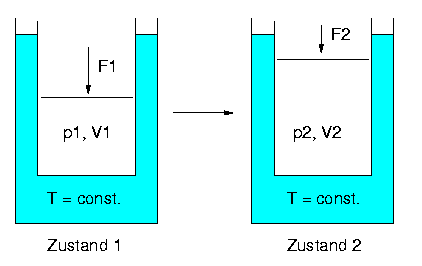
-
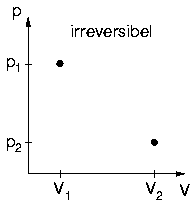
Prozess A: Übergang von Zustand 1 in Zustand 2 durch plötzliches
Verringern der Auflagekraft
- Gas dehnt sich plötzlich und turbulent
aus
- lokale Druckschwankungen
- lokale Temperaturänderungen durch Reibung
- keine Gleichgewichtszustände
-
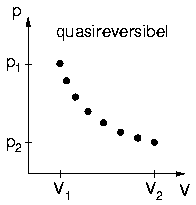
Prozess B: Übergang von Zustand 1 in Zustand 2 durch viele
winzige Zwischenschritte
- allmähliche Ausdehnung des Volumens
- lokale Ausgleichprozesse schnell gegen
Systemänderung
- interne Reibung vernachlässigbar
- Zwischenschritte lauter
Gleichgewichtszustände