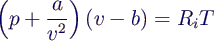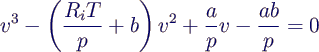Zustandsgleichungen realer Gase
-
Abweichung vom idealen Gas:
-
Realgasfaktor
-
als Funktion von p und T für Stickstoff
-
Van-der-Waals-Gleichung:
-
erweitert ideale Gasgleichung um zwei Korrekturterme
- Anziehungskräfte zwischen Molekülen
→ Druckkorrektur
- Eigenvolumen der Moleküle →
Volumenkorrektur
-
Damit
-
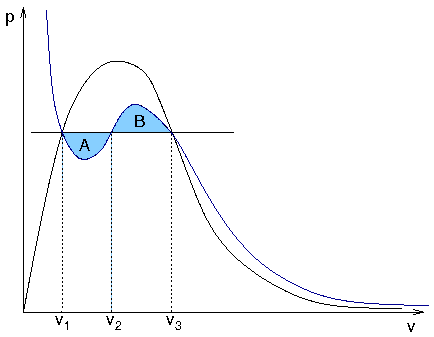
im p-V-Diagramm
-
geschrieben als Gleichung für v
-
für kleine Werte von p
- drei Lösungen
(v1,v2, v3 im Bild)
- Kurve unphysikalisch
- Flüssigkeit nicht
berücksichtigt
- Ersetzen durch gerade Linie, so dass
Flächen A und B gleich groß
-
für große Werte von p
- eine Lösung
- Grenzfall am kritischen Punkt
- kritische Temperatur: Wendepunkt mit
waagerechter Tangente
- damit:
- a = 3 pk
vk2
- b = vk/3
- Ri = 8 pk vk
/ (3 Tk)
-
Virialgleichung:
-
empirischer Ansatz
- p = RiT/v + B(T)/v2 +
C(T)/v3 + D(T)/v4 + ...
- B, C, D: Virialkoeffizienten
- viele andere Gleichungen zur näherungsweisen
Beschreibung realer Gase
- in der Praxis: Messwerte als Tabellen oder
Computerprogramme
-
Aufgaben: