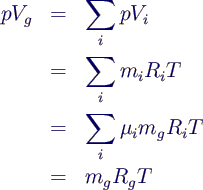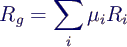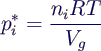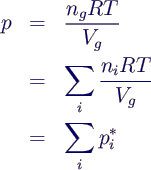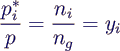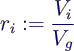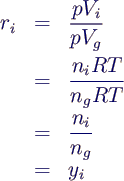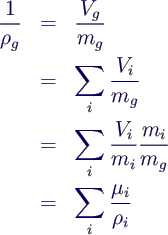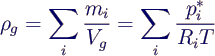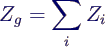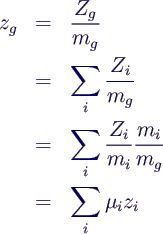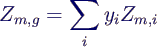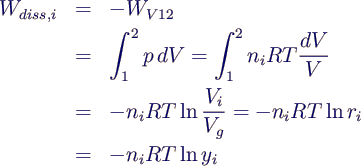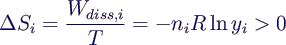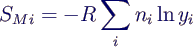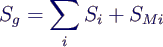Gemische idealer Gase
- Zustandsgleichung des Gemischs:
- ideale Gasgleichung der Komponenten vor der Mischung
- nach der Mischung p und T gleich
- Addition der Gleichungen →
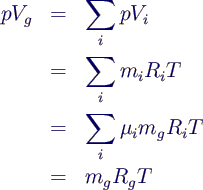
- mit Gaskonstante des Gemischs
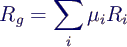
-
Partialdruck pi*:
- Komponente i nach Mischung auf Gesamtvolumen
Vg verteilt
- übt Teildruck (Partialdruck) pi*
aus mit
- Gesamtdruck p erfüllt
- Division liefert
- Volumen und Dichte:
-
Volumenanteil ri
- durch Molanteil gegeben wegen
- Dichte des Gemischs
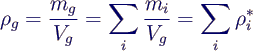
- mit den Partialdichten
ρi*
- aus den Massenanteilen bestimmt zu
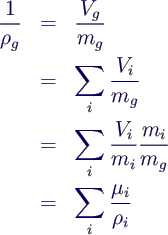
- mit den Dichten ρi bei gleichem
p und T
- mit der Gasgleichung für die Komponenten
- pi* Vg =
ni R T = mi Ri T
- gilt außerdem
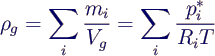
- Extensive Größen Zi:
- z.B. Enthalpie H, Wärmekapazitäten Cp,
CV
- addieren sich im Gemisch
- nicht Entropie (s.u.)
- bezogen auf Massen
- analog für molare Größen
- Entropie des Gemischs:
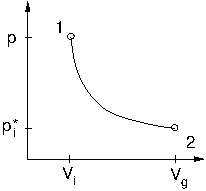
- Komponente i wird bei Mischung adiabatisch entspannt
- irreversibler, isothermer Prozess (Diffusion)
- Dissipationsenergie
- zugehörige Zunahme der Entropie
- Mischungsentropie über alle Komponenten
- Gesamtentropie des Gemischs
- Aufgaben: